药物名称:Vorasidenib(Voranigo)
适用症:IDH突变2级胶质瘤
近日,医学界迎来了一个振奋人心的消息——美国食品和药物管理局(FDA)正式批准了vorasidenib(Voranigo)作为治疗特定类型脑瘤的新药。这款药物专门针对携带异柠檬酸脱氢酶-1(IDH1)或异柠檬酸脱氢酶-2(IDH2)突变的II级星形细胞瘤和少突胶质瘤患者,为这些患者群体开启了新的治疗篇章。

图片来源:FDA官网
虽然II级星形细胞瘤和少突胶质瘤通常生长缓慢,但IDH1或IDH2基因的突变却使得这些肿瘤具有独特的生物学特性和治疗挑战。这些突变不仅促进了肿瘤细胞的生长,还影响了肿瘤微环境,使得传统治疗方法的效果有限。因此,针对这些突变的靶向治疗显得尤为重要。
Vorasidenib作为一种创新的靶向抑制剂,直接作用于IDH1和IDH2突变蛋白,阻断其异常功能,从而抑制肿瘤细胞的生长和扩散。在关键的INDIGO临床试验中,vorasidenib展现出了令人瞩目的疗效。
这项严谨的研究包括了331名接受手术治疗的II级星形细胞瘤或少突胶质瘤患者,他们被随机平分为两组,分别接受vorasidenib或安慰剂治疗。中位随访时间14.2个月后,226名患者(68.3%)继续接受vorasidenib或安慰剂治疗。
相较于安慰剂组,vorasidenib组在无进展生存期方面展现出了显著的改善,具体表现为中位无进展生存期延长至27.7个月,而安慰剂组仅为11.1个月。此外,vorasidenib组将疾病进展或死亡的风险降低了61%(危险比=0.39),这一结果具有高度的统计学显著性(P<0.001),其95%置信区间为0.27至0.56,进一步巩固了vorasidenib的积极疗效。
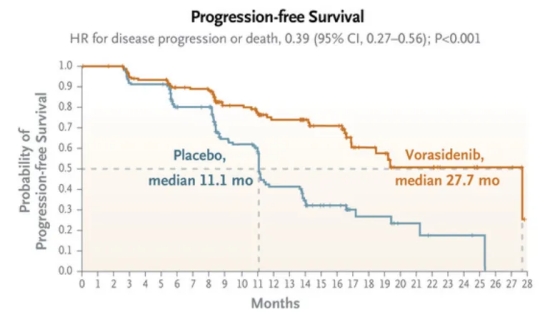
图片来源:DOI: 10.1056/NEJMoa2304194
同时,值得注意的是,与安慰剂组相比,vorasidenib组的患者在接受初始治疗后至下一次干预的时间间隔明显缩短,这一缩短的幅度由危险比0.26所量化,表明vorasidenib可能不仅延长了患者的无进展生存期,还可能在某种程度上加速了治疗反应或疾病监测的周期,为患者提供了更为及时的医疗干预机会。
当然,任何治疗都需要在确保安全的前提下进行。vorasidenib在治疗过程中虽然会出现一些不良反应,如疲劳、头痛等,但大多数反应都是可控且可管理的。此外,FDA为不同年龄和体重的患者制定了详细的剂量指导,确保每位患者都能获得适合自己的治疗方案。
Vorasidenib的审批过程也彰显了国际间在癌症治疗领域的紧密合作。FDA通过Project Orbis框架,与澳大利亚、巴西、加拿大、瑞士和以色列等多个国家的监管机构携手,共同推进这一创新药物的审评工作。这种跨国界的合作不仅加速了药物的上市进程,也为全球患者带来了更多的治疗机会。
内容来源:DOI: 10.1158/2159-8290.CD-24-0158
重要提示:本文所提供的所有与医疗相关的信息和建议,仅供读者参考和了解。对于任何医疗问题或疾病治疗,强烈建议读者务必遵循专业医生的诊断和建议,以确保安全和有效性。医疗决策应基于专业医生的评估和指导,本文内容不构成任何医疗建议或替代专业医疗意见。